近日,江苏大学材料学院博士研究生白蒙起(导师刘磊研究员)以第一作者在国际材料学权威期刊Advanced Materials上在线发表题为“A Bio-Inspired Free-Standing Film with Versatility: From Heterogeneous CTCs Programed Isolating to Breast Cancer Molecular Typing”的研究论文,江苏大学为该论文的第一单位和唯一通讯单位。

作为液体活检的重要临床标志物,循环肿瘤细胞(CTCs)的稀有性(正常血细胞中的十亿分之一)和表型异质性(不同的表面标记物)使癌症的精确诊断面临极大挑战。因此,将化学(分子识别),物理(微/纳米拓扑相互作用)与机械(柔性)作用相结合构建类细胞外基质(ECM)的“软”生物活性界面,识别并捕获具有不同表面标记物的CTCs并对其进行分选,对癌症的分子分型诊断意义重大。本论文开发了一种TiO2纳米管/丝素蛋白柔性复合膜,通过PDA化学和多重可逆共价相互作用将肿瘤细胞靶向生物标志物“上皮生物标志物”和“人上皮生长因子受体2”(HER2)固定在膜表面,以简单环保的方法制备了具有多重动态生物活性表面的TiO2纳米管/丝素蛋白柔性膜(TSF/MDBS)。柔性膜可以从癌症患者的未经处理的血液样本中捕获具有不同表型 (HER2+和HER2-)的CTCs,以区别HER2高表达或低表达,实验数据与术后免疫组织化学染色结果高度一致,检测准确率为100%,为今后癌症患者的预后和癌症患者的分子分型诊断提供依据。它还指导了多功能生物界面和智能复合膜的设计,可应用于多种生物医学领域。
镇江市第一人民医院医生秦蓉为论文的共同第一作者,江苏省人民医院徐建教授在临床诊断实验方面给予了大力帮助。
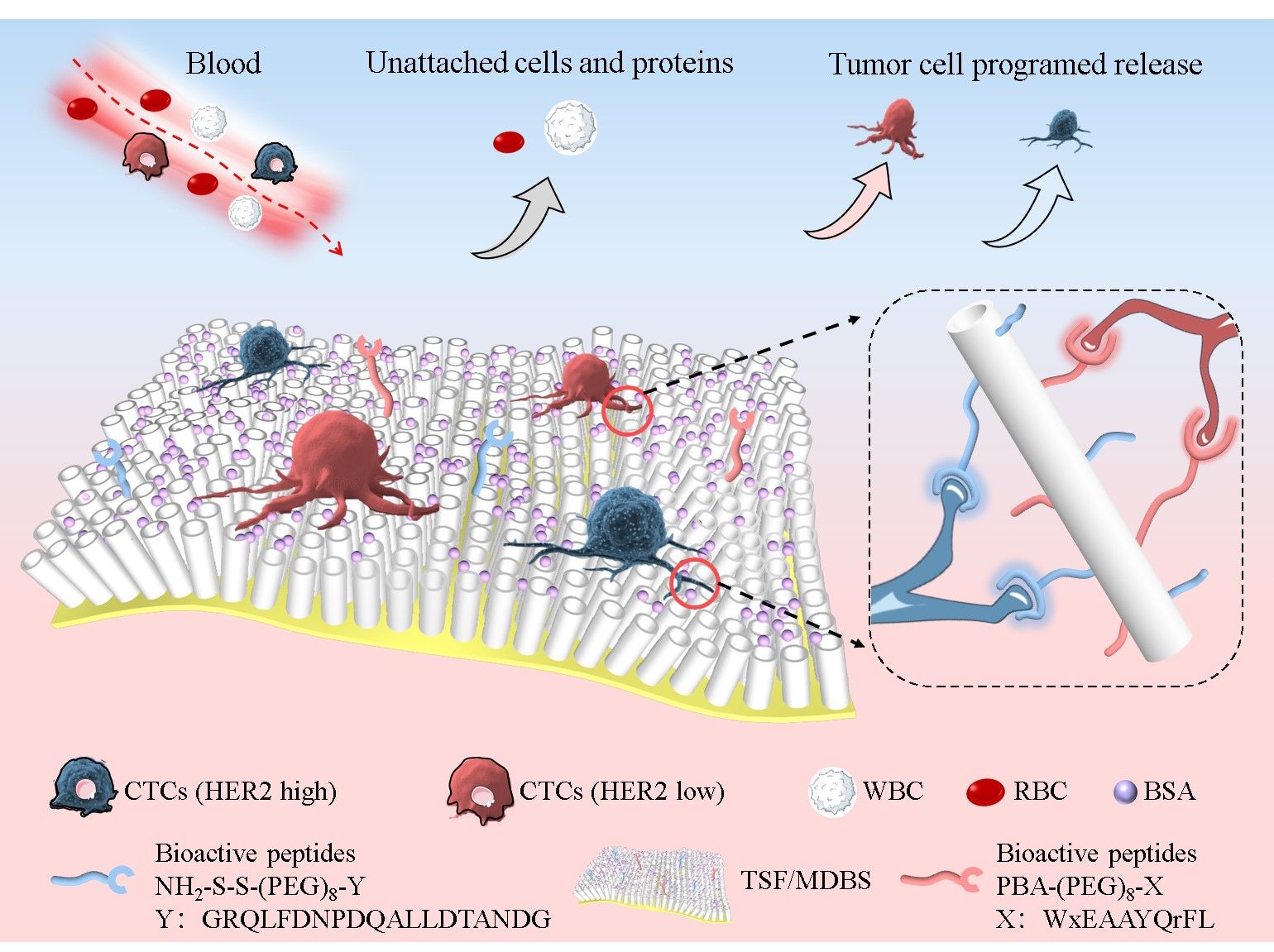
图1. TSF/MDBS捕获异质性CTCs的作用机理。
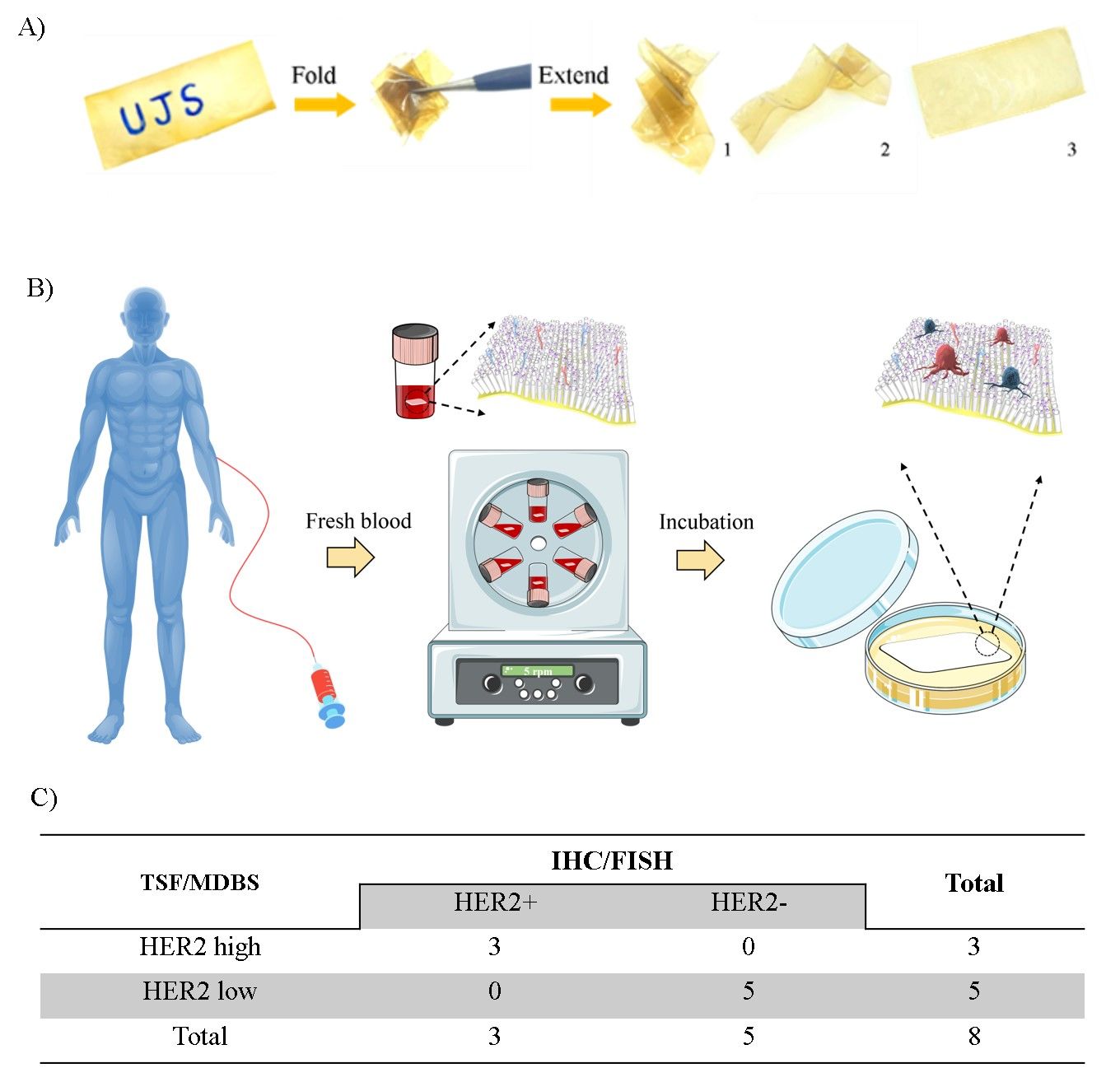
图2. A) TSF/MDBS实物图。B). 癌症病人血液样本中CTCs捕获的机理图示。C) 癌症病人血液样本中捕获的CTCs分类。
刘磊研究员团队围绕智能生物界面材料方向开展研究,近年来创建了具有动态生物活性的智能生物界面材料体系,用于循环肿瘤细胞的特异性捕获与分离。在此基础上,团队优化生物界面功能,实现对CTC快速无标记的灵敏检测,与此同时实现了全血中抗血液非特异黏附下的痕量肿瘤细胞的灵敏检测。近期,该团队在CTC液体活检研究中,利用功能生物界面克服了CTC的稀有性问题,进一步利用仿生柔性复合膜技术来攻克CTC的异质性给细胞检测带来的准确性低的难题。目前,团队正与江苏省人民医院合作,进入了大批量临床样本检测,希望该技术未来能用于临床肿瘤患者的分子分型诊断。
原文链接:https://doi.org/10.1002/adma.202309046